惗暔偲壔妛憃曽偱弌戣偝傟偆傞僌儖僞僠僆儞傪2夞偲傝偁偘傞丅
愝栤乮2003擭愮梩戝丒壔妛乯
丂僞儞僷僋幙偵斾傋偰彮悢偺兛傾儈僲巁偐傜側傞儁僾僠僪偵偼丄儂儖儌儞傗峈惗暔幙側偳偺傛偆偵惗棟妶惈傪桳偡傞傕偺偑偁傞丅
偨偲偊偽嵔忬偺僩儕儁僾僠僪偱偁傞僌儖僞僠僆儞偼摦怉暔偵峀偔懚嵼偟丄惗懱撪偺夝撆傗巁壔杊巭偵廳梫側摥偒傪墘偠偰偄傞丅
僌儖僞僠僆儞偼埲壓偵帵偟偨俈庬椶偺兛傾儈僲巁偺偆偪丄偄偢傟偐偱峔惉偝傟偰偄傞丅偨偩偟乮丂乯撪偼丄兛傾儈僲巁偺懁嵔傪帵偡丅
僌儕僔儞乮俫乯丂
傾儔僯儞乮CH3)
僙儕儞乮CH2OH)
僼僃僯儖傾儔僯儞乮CH2C6H5)
僔僗僥僀儞乮CH2SH)
僌儖僞儈儞巁乮CH2CH2COOH)
儕僔儞乮CH2CH2CH2CH2NH2)
僌儖僞僠僆儞傪峔惉偡傞兛傾儈僲巁傪寛掕偡傞偨傔丄埲壓偺憖嶌傪峴偭偨丅
憖嶌侾
丂僌儖僞僠僆儞傪巁偱姰慡偵壛悈暘夝偟偨偲偙傠丄俁庬椶偺兛傾儈僲巁偑惗惉偟偨丅
偙傟傜俁庬椶偺兛傾儈僲巁偺摍揹揰偼丄偦傟偧傟
5丆97丄
5丆07丄
3丆22丄
偱偁偭偨丅
丂傑偨偙偺偆偪堦偮偺兛傾儈僲巁偼晄惸扽慺尨巕傪傕偨側偐偭偨丅
憖嶌俀
丂僌儖僞僠僆儞傪庛偄巁偱晹暘揑偵壛悈暘夝偟偨偲偙傠丄俀庬椶偺僕儁僾僠僪A偲B偑惗惉偟偨丅
A偲B偵擹偄悈巁壔僫僩儕僂儉悈梟塼傪壛偊偨屻丄恷巁墧乮俀乯悈梟塼傪壛偊傞偲丄偄偢傟傕崟怓捑揳偑惗偠偨丅
栤侾丂憖嶌侾傛傝丄僌儖僞僠僆儞偵娷傑傟傞兛傾儈僲巁偺偆偪俀庬椶傪摿掕偡傞偙偲偑偱偒傞丅俀庬椶偺兛傾儈僲巁偺柤徧偲棟桼傪婰偣丅
栤俀丂憖嶌俀偱惗偠偨崟怓捑揳偺壔妛幃傪彂偒側偝偄丅
栤俁丂憖嶌俀傛傝丄僌儖僞僠僆儞偵偼丄憖嶌侾偱柧傜偐偵側偭偨俀庬椶偺兛傾儈僲巁埲奜偵偳偺兛傾儈僲巁偑娷傑傟偰偄傞偙偲偑傢偐傞偐丅
栤係丄偦偺屻偺幚尡偵傛傝丄僌儖僞僠僆儞偱偼懁嵔R偵娷傑傟傞姱擻婎偑儁僾僠僪寢崌乮傾儈僪寢崌乯偵
娭梌偟偰偄傞偙偲偑柧傜偐偵側偭偨丅
僌儖僞僠僆儞偺梊應偝傟傞峔憿幃傪彂偒側偝偄丅
伀
伀
乮峫偊傞乯
伀
伀
伀
摎
栤侾丂僌儕僔儞乮晄惸扽慺偑側偄偺偱乯
丂丂丂僌儖僞儈儞巁乮摍揹揰偑掅偄乮巁惈懁偵偁傞乯巁惈傾儈僲巁偼僌儖僞儈儞巁偺傒側偺偱乯
栤俀丂俹bS乮娷棸傾儈僲巁乽僔僗僥僀儞丒儊僠僆僯儞乿偲懁嵔偺棸墿偲斀墳乯
栤俁丂僔僗僥僀儞
栤係丂壓恾偑摎
丂
憖嶌俀偱椉抐曅偲傕偵棸墿斀墳傪婲偙偟偰偄傞偺偱拞墰偺傾儈僲巁偑僔僗僥僀儞偲傢偐傞丅
乽懁嵔偑儁僾僠僪寢崌偵娭梌乿偲彂偄偰偁傞偑懁嵔偵儁僾僠僪寢崌偵娭梌偑壜擻側傾儈僲巁偼僌儖僞儈儞巁乮COOH偁傝乯丄
儕僔儞乮NH2偁傝乯側偳偱偁傞偑丄慜偺婰弎偐傜僌儖僞儈儞巁偲傢偐傞丅
偟偨偑偭偰
乽僌儖僞儈儞巁乕懁嵔偺COOH偱寢崌乕僔僗僥僀儞乕僌儕僔儞乿偲傢偐傞丅
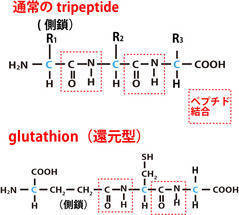
仠捠忢偺僩儕儁僾僠僪偼挬偺僕傌僾僠僪偲摨條丄忋恾偺傛偆偵懁嵔偑偦傟偧傟拞怱扽慺偐傜攈惗偟丄儁僾僠僪寢崌偵偼娭梌偟側偄丅
偟偐偟丄椺奜傕偁傞丅
捠忢偺拞怱偺扽慺尨巕乮恾偱惵帤偱昞婰乯
偵寢崌偡傞NH2偲COOH偳偆偟偑儁僾僠僪寢崌偡傞偱側偔丄
懁嵔偺NH2傗COOH偑儁僾僠僪寢崌偵娭梌偡傞偲偄偆摿庩偩偑桳柤側椺偑乽僌儖僞僠僆儞乿側偺偱梫拲堄丅
尩枾偵偼偙傟偼娨尦宆僌儖僞僠僆儞乮GSH乯丅偦偺堄枴偼柧擔偵丅