細胞の情報伝達において「タンパク質リン酸化」(それを行う酵素が〇〇キナーゼ)が重要です。それは化学的な現象でもあり、化学でも出題されます。まず今日は化学的におさえ、明日生物学的におさえましょう。
★設問(2001年信州大/化学/部分)
カゼインキナーゼという酵素は、乳腺細胞のゴルジ体において、(1)「α―アミノ酸だけからできているタンパク質」の
(2)「セリンやトレオニンと呼ばれるアミノ酸の側鎖のヒドロキシル基にリン酸が脱水縮合反応する」
のを触媒する。
しかし、カゼインキナーゼはチロシンと名づけられたアミノ酸の側鎖のヒドロキシル基にリン酸が
脱水縮合反応するのを触媒することはできない。このことから、カゼインキナーゼの基質特異性はセリンとトレオニンにある。
一方、カゼインキナーゼの基質特異性は、リン酸の脱水縮合反応を受けるアミノ酸の種類によってだけでなく、
セリンやトレオニンの2つ後にくるアミノ酸の種類によっても支配される。すなわち、
カゼインキナーゼは、タンパク質に存在する[セリンまたはトレオニン]―A―[グルタミン酸またはアスパラギン酸]という
アミノ酸配列のセリンやトレオニンにリン酸が脱水縮合反応するのを触媒する
(−はペプチド結合を、Aは不特定アミノ酸を示す)。
なお、カゼインキナーゼによるリン酸の脱水縮合反応の反応速度は、
トレオニンを基質としたときよりもセリンを基質としたときの方が速く、
また、セリンやトレオニンの2つ後にくるアミノ酸はアスパラギン酸のときよりもグルタミン酸のときの方が速い。
問1 (1)「α―アミノ酸だけからできているタンパク質」は一般に、何と呼ばれるタンパク質か。
↓
↓
↓
(考える)
↓
↓
(答)
単純タンパク質
注、ここで画面を止めてください。
次の設問の資料が画面の上側に画像でありますが、
メルマガの都合上、その画像のすぐ下に答があります。
したがって皆様は画面の下の方を手で隠しながら、
まず画像の上側を見て考えたのちに下側の答をみてください。
問2 セリンとリン酸の構造式は以下のようである。これに続けてセリン側鎖とリン酸の脱水縮合反応の化学反応式の後半を縮合反応生成物については構造式で書け。
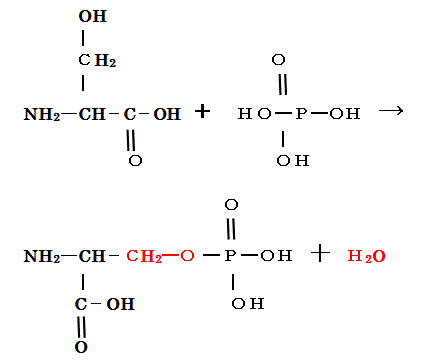
COOHとNH2はペプチド結合し、側鎖とはならない。リン酸化は側鎖であるし、問2にも「セリン側鎖」と明記されているので、COOHのOHをリン酸化しないように注意。
(出題者が「いじわる」にCOOHをリン酸のそばに書いてあるがひっかからないように・・・)
★解説
すでにシグナル伝達でタンパク質のリン酸化は非常に重要だと解説したが、あらためて分子的レベルで確認したい。
リボソームで翻訳されたタンパク質は、翻訳後修飾でリン酸化(タンパク質リン酸化protein phosphorylation)され
活性型酵素など活性型タンパク質になることがある。逆にリン酸化後、脱リン酸化されると活性が失われる(比率は少ないが逆の場合―脱リン酸化で活性化、リン酸化で不活性化―もある)。
タンパク質リン酸化酵素(protein kinaze、キナーゼ)はヒトでは1000種類あり細胞内タンパク質の10%はリン酸化されている。
なお脱リン酸化して不活性化する酵素を「フォスファターゼ」という。
リン酸化はタンパク質のアミノ酸(残基)のうち側鎖にOHのあるセリン・トレオニン・チロシン(残基)のOH基に起きる縮合重合(脱水縮合)である。(他のアミノ酸残基におきることも少数ある)
「OHさん(王さん)とリン酸(林さん)が結婚する」
とおさえましょう。セリンとトレオニンは側鎖の反応部位の分子構想が類似し(メチル基CH3のみ相違)、
「セリン/トレオニンプロテインキナーゼ」と分類される酵素群が反応する。チロシンは大きなベンゼン環が存在し分子構造が異なり、「チロシンプロテインキナーゼ」と分類される別の酵素群が反応する。
★側鎖にOHを持ち、リン酸化されやすいのは
「トレオニン・セリン・チロシン」〜そのおさえ方〜
これは知識としては聞かれることはないので、おさえておく必要はないとはいえ、パッとわかると便利なので無理やりおさえ方をこじつけました。
私昔、牛丼吉野家で、朝定食(納豆・焼魚定食)の補助要員としてバイトしていました。
朝6時の定食時間になるとお客さんが大量に押し寄せるので、
その前にカウンター脇に定食用のトレイを設置しておきます。
ということで
「(納豆定食の)トレーを設置」で
「トレ」オニン・「セ」リン・「チ」ロシン
★頻度は少ないと考えてよいが、側鎖カルボキシル基のOHや他の部位がリン酸化されることもある。
側鎖にカルボキシル基を持つのは
アスパラギン酸・グルタミン酸ですが
CーOH
‖
О
なのでそのOH部分がリン酸化されることもあります。
(2007京都府立医大/化学出題 )